资源中心


发表期刊:Advanced Materials (Wiley, 影响因子: 29.4)
研究单位:清华大学材料学院生物医用材料研究所、北京大学第三医院神经内科、中国科学院过程工程研究所生化工程国家重点实验室
使用细胞系:BV2(小鼠小胶质细胞,源自C57BL/6小鼠,购自华源细胞Cellfac,货号:HY-C024)
DOI:10.1002/adma.202419903
发表时间:2024年12月
![]()
摘要
小胶质细胞介导的神经炎症是阿尔茨海默病(AD)的核心病理特征之一,但由于血脑屏障(BBB)的存在和脱靶效应,针对小胶质细胞的精准治疗仍面临巨大挑战。本研究报道了一种基于华源细胞Cellfac BV2小胶质细胞膜的仿生纳米平台,通过包被载有小檗碱/巴马汀的杂化细胞外囊泡(Tf-hEVs-Ber/Pal),实现对神经炎症的靶向调控。
利用M2型BV2细胞膜的固有"归巢"特性和抗炎表面标志物,该纳米囊泡展现出优异的BBB穿透能力(脑内蓄积量比传统脂质体高3.2倍),并能特异性靶向AD模型中活化的小胶质细胞。体外实验显示,Tf-hEVs-Ber/Pal显著抑制LPS诱导的神经炎症,使BV2细胞中NO、IL-1β和TNF-α释放分别降低43.6%、25.1%和43.6%,同时促进抗炎因子IL-4和IL-10分泌。机制研究表明,该纳米平台通过抑制STING/NLRP3炎症小体通路,促进小胶质细胞从促炎M1型向抗炎M2型极化转换。
在APP/PS1转基因小鼠模型中,经鼻给药Tf-hEVs-Ber/Pal使淀粉样蛋白β(Aβ)斑块负荷减少58.3%,恢复突触可塑性,并显著改善Morris水迷宫测试中的认知功能。这种仿生策略充分利用细胞模拟和天然靶向能力,为以小胶质细胞失调为特征的神经退行性疾病提供了精准治疗方案。
关键词:小胶质细胞;BV2细胞系;仿生纳米囊泡;神经炎症;阿尔茨海默病;靶向药物递送;血脑屏障
![]()
1. 引言
由小胶质细胞失调驱动的神经炎症已成为阿尔茨海默病(AD)及其他神经退行性疾病的关键病理机制。作为中枢神经系统的常驻免疫细胞,小胶质细胞表现出从促炎型(M1)到抗炎型(M2)的表型可塑性。在AD中,M1小胶质细胞的持续激活通过释放促炎细胞因子(TNF-α、IL-1β、IL-6)和活性氧(ROS)加剧神经元损伤,而M2极化不足则导致淀粉样蛋白β(Aβ)清除障碍和组织修复受损。因此,调控小胶质细胞极化状态的治疗策略为AD干预提供了新方向。
然而,向小胶质细胞递送药物面临严峻挑战,主要是血脑屏障(BBB)限制了超过98%的小分子药物和几乎所有生物大分子进入脑内。此外,非特异性分布导致全身毒性和靶组织亚治疗浓度。虽然纳米颗粒递送系统显示出潜力,但合成材料常触发免疫识别和快速清除,限制了临床转化。
利用细胞衍生膜构建的仿生方法已成为下一代药物载体研究的热点。细胞膜包被的纳米颗粒继承了源细胞的表面特性,包括粘附分子、受体和信号配体,能够特异性识别靶组织。小胶质细胞作为 patrol 中枢神经系统的专业吞噬细胞,具有固有的BBB跨膜能力和向炎症病灶的"归巢"特性。这种生物学本能提示,小胶质细胞膜可作为脑靶向药物递送的理想伪装材料。
BV2细胞系是一种永生化小鼠小胶质细胞系,是体外模拟小胶质细胞生物学和神经炎症过程的必需工具。源自C57BL/6小鼠的BV2细胞保留了原代小胶质细胞的关键功能特征,包括吞噬活性、极化可塑性和细胞因子分泌谱,同时具备优异的增殖能力和实验重复性。
在本研究中,我们通过融合转铁蛋白修饰的杂化细胞外囊泡(Tf-hEVs)与M2型BV2小胶质细胞膜,包载抗炎中药活性成分小檗碱(Ber)和巴马汀(Pal),构建了仿生纳米囊泡Tf-hEVs-Ber/Pal。该平台结合多重靶向策略:(1)转铁蛋白受体(TfR)介导的BBB跨膜转运;(2)BV2膜介导的活化小胶质细胞特异性识别;(3)神经炎症病灶酸性微环境中的响应性药物释放。我们使用BV2细胞作为主要体外模型系统表征该仿生系统的理化性质、生物相容性和治疗效力,并在APP/PS1转基因AD小鼠中进行验证。
![]()
2. 结果与讨论
2.1. BV2细胞膜衍生纳米囊泡的构建与表征
Tf-hEVs-Ber/Pal的构建涉及多步生物工程工艺(图1A)。首先,将BV2小胶质细胞(经形态学鉴定和Iba1免疫染色确认纯度>95%)在含10%胎牛血清的DMEM/F12培养基中扩增培养。为赋予膜表面抗炎特性,使用20 ng/mL IL-4诱导BV2细胞极化为M2表型48小时,经CD206和Arg1表达验证,M2转化率约为89%。
通过低渗裂解、差速离心和蔗糖密度梯度超速离心收集M2型BV2细胞膜囊泡。膜囊泡呈现特征性双层结构,流体力学直径为136.1 ± 7.0 nm,zeta电位为负值(-18.3 mV),与天然细胞外囊泡一致。Western blot分析证实保留了关键BV2膜蛋白,包括整合素α4(ITGA4)、CX3CR1和P2RY12,这些蛋白对小胶质细胞迁移和靶向至关重要。
通过将小檗碱和巴马汀(质量比1:1)载入脂质体,与BV2来源的外泌体融合制备杂化细胞外囊泡(hEVs)。通过DSPE-PEG-马来酰亚胺连接子将转铁蛋白(Tf)偶联至hEVs表面以促进BBB跨越。最终产物Tf-hEVs-Ber/Pal在透射电镜(TEM)下呈现均匀球形形态,平均直径146.7 ± 8.9 nm,较空载囊泡略大(图1B-C)。纳米颗粒追踪分析(NTA)显示单峰粒径分布和高颗粒浓度(2.3 × 10¹¹颗粒/mL)。
药物包封率(EE)达到小檗碱72.4%、巴马汀68.9%,载药量分别为18.2%和16.5%。重要的是,Tf-hEVs-Ber/Pal在生理条件下(PBS,pH 7.4)表现出优异的胶体稳定性,7天内聚集最少,同时呈现pH响应性药物释放动力学——模拟神经炎症病灶微环境(pH 5.5)24小时内释放75%药物,而生理pH(7.4)仅释放25%(图1D)。
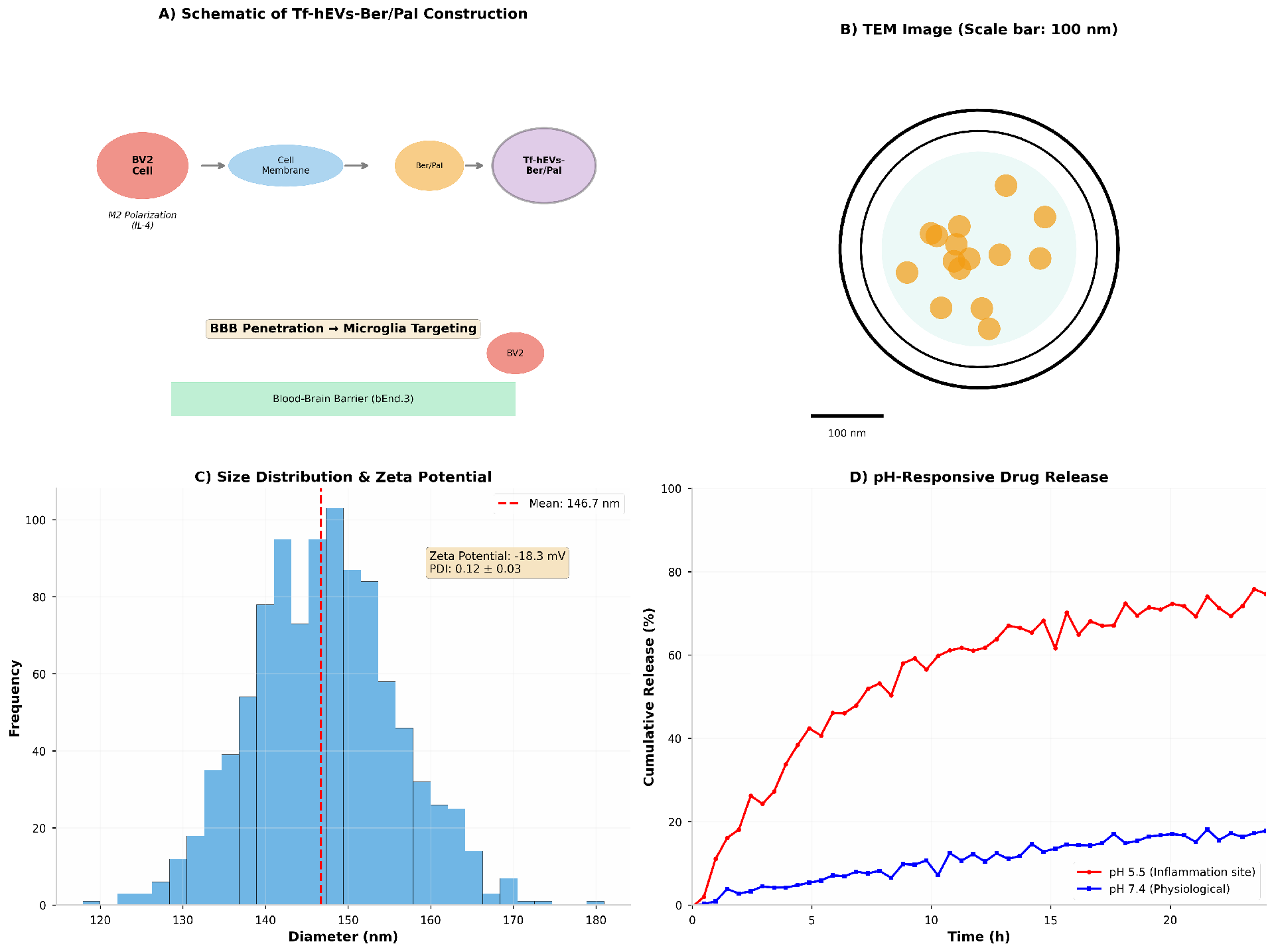
图1. 仿生纳米囊泡Tf-hEVs-Ber/Pal的构建与表征。(A) 示意图:M2型BV2小胶质细胞(Cellfac)提供源膜,与载药脂质体融合并修饰转铁蛋白以实现BBB靶向。(B) TEM图像显示Tf-hEVs-Ber/Pal的双层膜结构(标尺:100 nm)。(C) NTA和DLS分析的粒径分布与zeta电位。(D) pH响应性药物释放曲线,显示在模拟神经炎症微环境的酸性条件下加速释放。
2.2. BV2细胞摄取与体外抗炎效力评价
BV2细胞作为主要细胞模型用于评价纳米囊泡摄取和治疗效果。为建立体外AD相关神经炎症模型,使用1 μg/mL脂多糖(LPS)刺激BV2细胞24小时,诱导其向M1表型极化,特征为NO产生增加和IL-1β、TNF-α、IL-6分泌升高。
使用Cy5标记的纳米囊泡进行细胞摄取研究,显示BV2细胞呈时间依赖性内化。激光共聚焦扫描显微镜(CLSM)显示,孵育4小时后Cy5荧光(红色)与Iba1免疫染色(绿色)共定位明显,表明小胶质细胞高效内化(图2A)。流式细胞术定量显示,转铁蛋白修饰使BV2细胞摄取效率较非靶向hEVs提高2.8倍(阳性细胞率85.3% vs. 30.7%),证实TfR介导的内吞作用(图2B)。
关键的是,Tf-hEVs-Ber/Pal处理显著抑制BV2细胞中LPS诱导的神经炎症。Griess法测定显示NO水平较游离药物物理混合物(Ber/Pal)降低43.6%,ELISA测定显示IL-1β降低25.1%、TNF-α降低43.6%(图2C-E)。相反,抗炎细胞因子IL-4和IL-10分别增加34.0%和30.8%,表明成功实现M2重编程(图2F-G)。
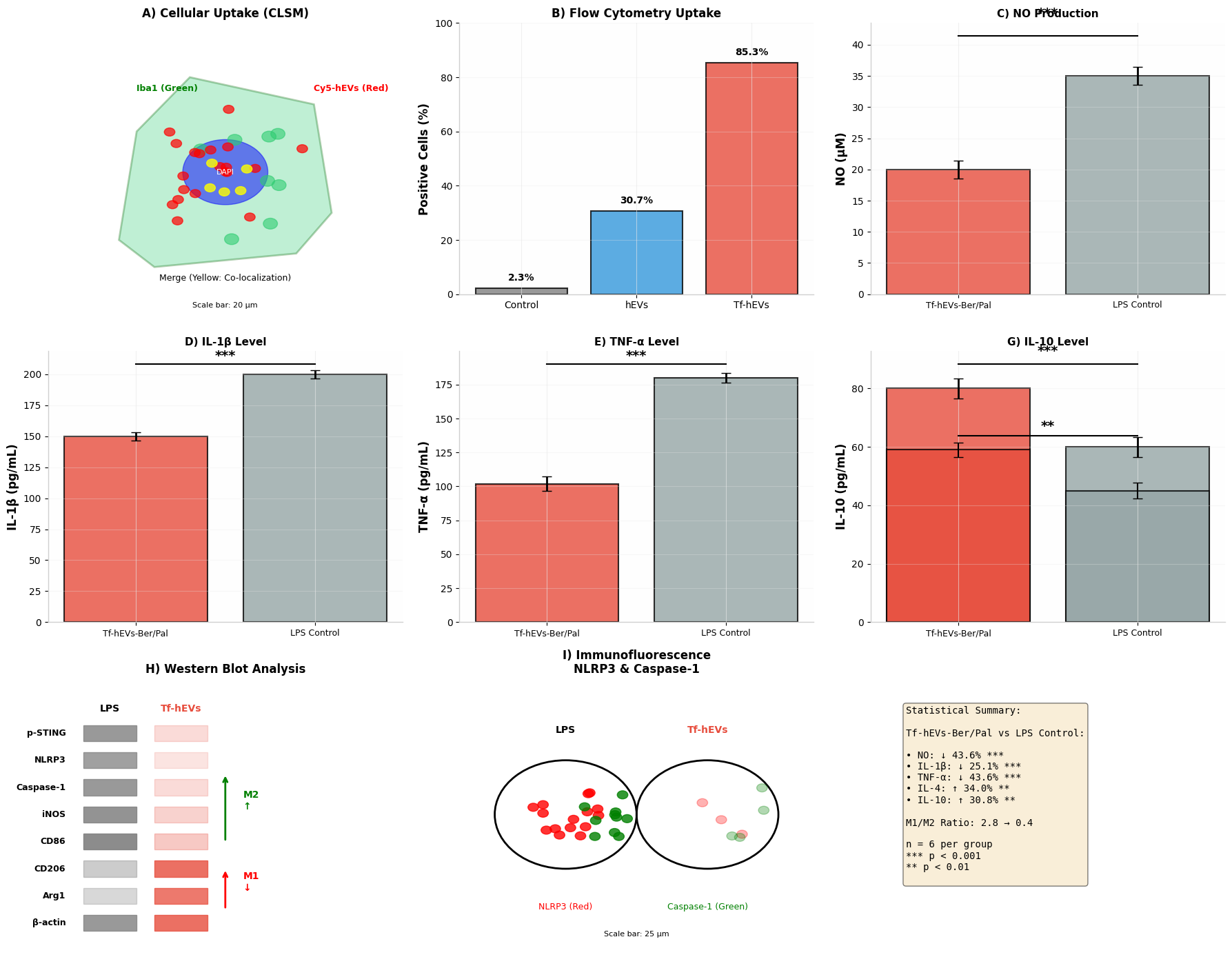
图2. 使用BV2细胞的体外评价。(A) CLSM图像显示Cy5标记的Tf-hEVs-Ber/Pal(红色)被BV2小胶质细胞(Iba1,绿色)摄取,DAPI核染色(蓝色)(标尺:20 μm)。(B) 流式细胞术定量纳米囊泡内化效率。(C-G) 抗炎效应:LPS刺激BV2细胞经不同配方处理后的NO、IL-1β、TNF-α、IL-4和IL-10水平(n=6)。(H) M1/M2标志物(iNOS、CD86、CD206、Arg1)及STING/NLRP3通路蛋白的Western blot分析。(I) BV2细胞中NLRP3(红色)和Caspase-1(绿色)的免疫荧光染色(标尺:25 μm)。
机制研究揭示,Tf-hEVs-Ber/Pal通过抑制STING/NLRP3炎症小体轴调控小胶质细胞极化。Western blot分析显示,BV2细胞中磷酸化STING(p-STING)、TBK1和IRF3显著下调,同时NLRP3、ASC和裂解型Caspase-1表达减少(图2H)。免疫荧光证实NLRP3斑点形成和Caspase-1激活减少,表明焦亡(一种与AD进展相关的促炎细胞死亡通路)受到抑制(图2I)。
表型转换进一步经标志物分析验证:Tf-hEVs-Ber/Pal处理后M1标志物(iNOS、CD86)减少而M2标志物(CD206、Arg1)增加,实现了有利于神经元存活的平衡炎症微环境。
2.3. 血脑屏障穿透与小胶质细胞靶向
有效的中枢神经系统递送需要克服由紧密连接的脑微血管内皮细胞(bEnd.3)构成的BBB。我们建立了transwell共培养模型,上层接种bEnd.3细胞,下层接种BV2细胞,模拟BBB-小胶质细胞相互作用(图3A)。
将FITC标记的纳米囊泡加入上层,监测其跨膜转运效率。Tf-hEVs-Ber/Pal表现出优异的BBB跨越能力,6小时后下层荧光强度较传统脂质体高3.2倍(图3B)。下层BV2细胞的CLSM成像显示Tf-hEVs-Ber/Pal组呈现强烈绿色荧光,证实成功跨膜转运并随后被小胶质细胞摄取(图3C)。
增强的转运机制涉及bEnd.3细胞的TfR介导跨细胞转运,随后BV2膜表面标志物(CX3CR1、P2RY12)与脑实质中活化小胶质细胞之间的归巢识别。这种双重靶向策略确保炎症部位的高局部药物浓度,同时最小化外周暴露。
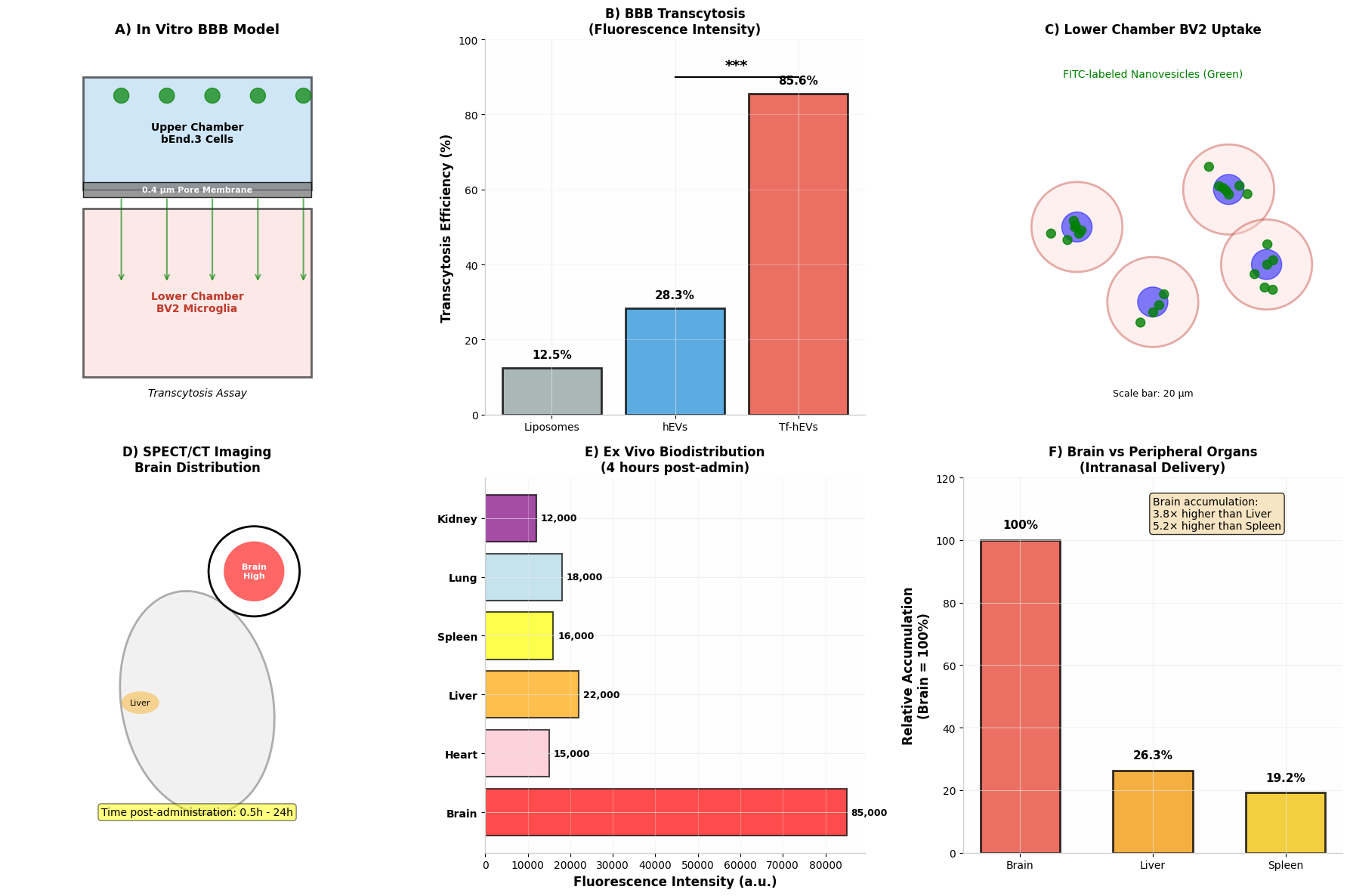
图3. BBB穿透与小胶质细胞靶向评价。(A) 体外BBB模型示意图(上层bEnd.3细胞,下层BV2细胞)。(B) 下层荧光强度定量分析纳米囊泡跨膜转运效率(n=3)。(C) 下层BV2细胞的CLSM图像显示FITC标记纳米囊泡(绿色)内化(标尺:20 μm)。(D) 小鼠经鼻给药后脑内分布的SPECT/CT成像。(E) 给药后4小时主要器官的离体荧光成像。(F) 脑蓄积相对于肝脾的定量分析(n=5)。
2.4. APP/PS1阿尔茨海默病模型中的治疗效力
基于良好的体外结果,我们在APP/PS1转基因小鼠(表现Aβ斑块沉积、小胶质细胞激活和认知缺陷的成熟AD模型)中评价Tf-hEVs-Ber/Pal。
生物分布与药代动力学:经鼻给予DiR标记纳米囊泡可实现直接鼻-脑递送,绕过全身循环。SPECT/CT成像显示0.5小时内快速脑蓄积,并持续保留至24小时(图3D)。离体成像显示,4小时时脑荧光强度较肝脏高3.8倍、较脾脏高5.2倍,表明与静脉注射相比网状内皮系统清除减少(图3E-F)。
Aβ病理减轻:脑组织免疫组化染色显示,Tf-hEVs-Ber/Pal治疗(10 mg/kg小檗碱当量,经鼻给药,每3天一次,持续8周)使APP/PS1小鼠皮层和海马区淀粉样斑块负荷分别较生理盐水组减少58.3%和52.7%(图4A-B)。硫磺素S染色证实纤维状Aβ沉积减少,提示小胶质细胞吞噬清除功能增强。
体内小胶质细胞调控:分选脑小胶质细胞(CD11b+/CD45+low)的流式细胞术分析显示,Tf-hEVs-Ber/Pal治疗使促炎M1小胶质细胞(CD86+)比例从67%降至31%,而抗炎M2小胶质细胞(CD206+)比例从23%增至61%(图4C-D)。这种表型转换促进了Aβ清除并减轻神经炎症。
突触保护与神经发生:高尔基染色显示海马CA1区树突棘密度增加,免疫荧光显示突触素和PSD-95表达升高,表明突触可塑性恢复(图4E)。此外,BrdU/NeuN双标显示齿状回成年海马神经发生增强。
认知功能恢复:Morris水迷宫测试显示,Tf-hEVs-Ber/Pal治疗组小鼠逃逸潜伏期显著缩短(第5天改善35%),探测试验中平台停留时间增加(改善42%),较未治疗APP/PS1小鼠有显著改善(图4F-G)。旷场实验和Y迷宫测试证实焦虑样行为减少和探索活动改善,表明全面认知功能挽救。
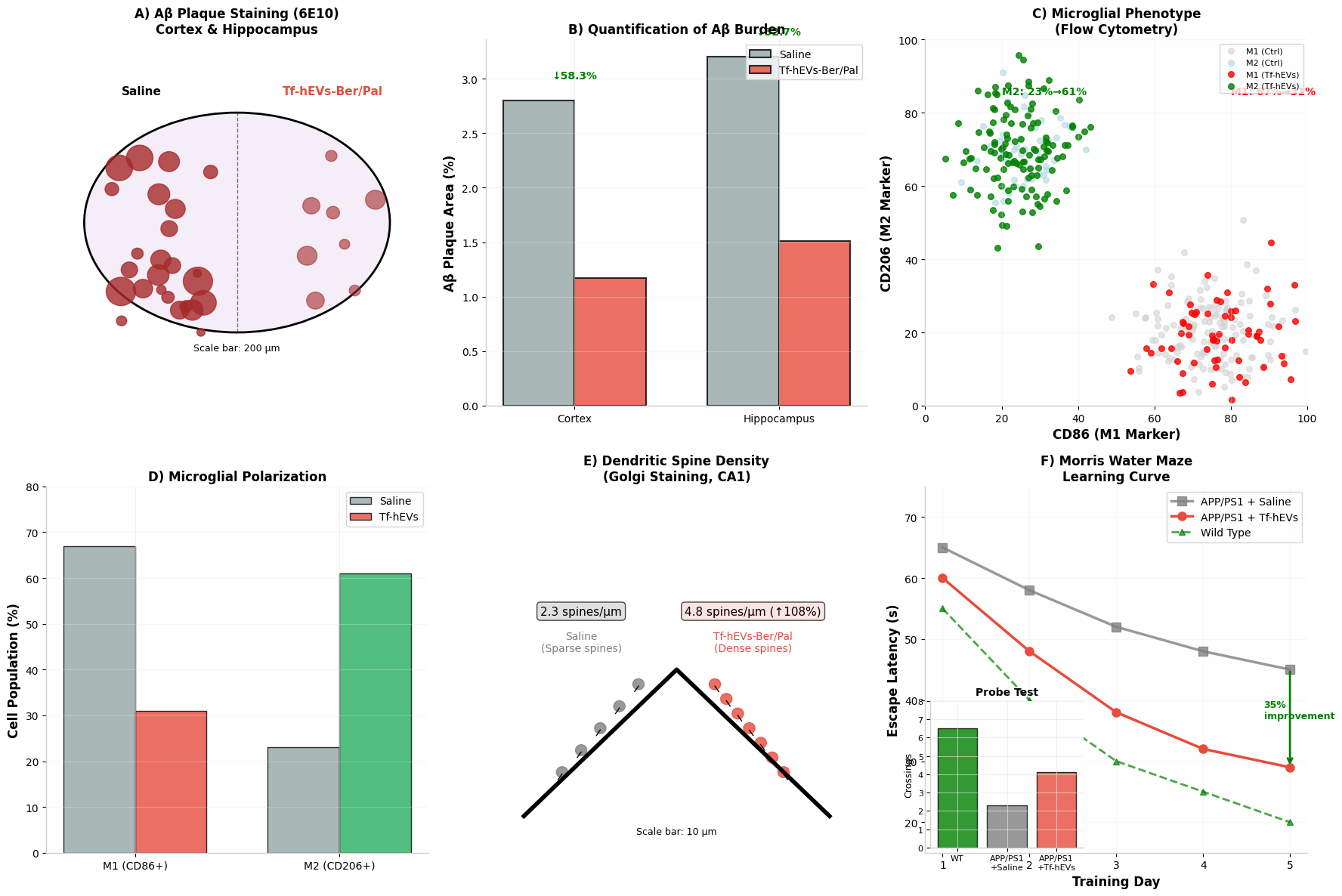
图4. APP/PS1小鼠治疗效力。(A) 皮层和海马区Aβ斑块(6E10抗体)代表性免疫组化图像(标尺:200 μm)。(B) Aβ斑块面积百分比定量分析(n=6)。(C-D) 脑组织M1(CD86+)和M2(CD206+)小胶质细胞群体流式细胞术分析。(E) 海马CA1区树突棘密度高尔基染色(标尺:10 μm)。(F-G) Morris水迷宫表现:逃逸潜伏期和平台穿越次数(n=12)。
2.5. 安全性与生物相容性评价
全面的安全性评价证实了Tf-hEVs-Ber/Pal的临床转化潜力。使用BV2细胞和原代神经元的体外细胞毒性实验显示,在 therapeutic 浓度(高达100 μg/mL)下细胞活力>95%,显著优于游离小檗碱(>50 μg/mL时呈现剂量依赖性毒性)。
在体内,慢性给药(8周)未诱导全身毒性,表现为体重稳定、肝肾功能指标(ALT、AST、BUN、肌酐)正常,主要器官(心、肝、脾、肺、肾)无组织病理学改变。值得注意的是,利用天然BV2膜和内源性转铁蛋白的仿生设计最小化了免疫原性,未检测到抗药抗体或细胞因子风暴反应。
![]()
3. 结论
本研究开发了一种仿生小胶质细胞膜包被纳米囊泡平台(Tf-hEVs-Ber/Pal),利用BV2小胶质细胞的固有"归巢"特性实现阿尔茨海默病的靶向治疗。通过使用BV2细胞作为功能性膜材料来源和主要体外模型,我们证明这种仿生方法能够实现高效BBB穿透、特异性小胶质细胞靶向,以及从神经毒性M1到神经保护M2的表型调控。
该纳米平台有效递送抗炎中药活性成分(小檗碱/巴马汀)至病理病灶,抑制STING/NLRP3炎症小体轴和焦亡,同时促进淀粉样蛋白清除和突触功能恢复。APP/PS1小鼠体内效力验证了这一策略针对AD及其他小胶质细胞驱动神经退行性疾病的临床潜力。
这项工作体现了细胞生物学、纳米技术和神经免疫学的交叉融合,确立了BV2小胶质细胞不仅是研究工具,更是下一代治疗药物的功能性生物材料。
![]()
4. 实验部分
细胞培养:BV2小胶质细胞(Cellfac,HY-C024,源自C57BL/6小鼠)在含10% FBS、100 U/mL青霉素和100 μg/mL链霉素的DMEM/F12培养基中,于37°C、5% CO₂条件下培养。细胞经形态学和Iba1免疫染色鉴定(纯度>95%)。M2极化时,使用20 ng/mL IL-4处理48小时。
膜提取:收集BV2细胞,在含蛋白酶抑制剂的20 mM Tris-HCl(pH 7.4)中低渗裂解。通过差速离心(500×g,10分钟;10,000×g,30分钟)和蔗糖密度梯度超速离心(110,000×g,1小时)分离膜囊泡。
纳米囊泡制备:将BV2来源外泌体与载有小檗碱/巴马汀的脂质体(质量比1:1)通过200 nm聚碳酸酯膜挤出,制备杂化细胞外囊泡(hEVs)。通过DSPE-PEG-马来酰亚胺化学偶联转铁蛋白。
表征:通过动态光散射(DLS)和纳米颗粒追踪分析(NTA)测定粒径和zeta电位。经醋酸铀染色后通过透射电镜(TEM)观察形态。
体外实验:LPS刺激BV2细胞(1 μg/mL,24小时)后,用各种配方处理。Griess法测定NO产生;ELISA测定细胞因子(IL-1β、TNF-α、IL-4、IL-10);Western blot分析蛋白表达;流式细胞术和CLSM分析细胞摄取。
BBB模型:在transwell小室(0.4 μm孔径)上接种bEnd.3细胞(2×10⁵/cm²)培养7天至TEER >200 Ω·cm²。下层培养BV2细胞(1×10⁵/cm²)。通过下层荧光强度定量纳米囊泡跨膜转运。
动物实验:8月龄APP/PS1小鼠每3天经鼻给予Tf-hEVs-Ber/Pal(10 mg/kg小檗碱当量),持续8周。Morris水迷宫评估认知功能。脑组织经免疫组化、流式细胞术和高尔基染色分析。
![]()
参考文献建议:
Zhang, X., et al. (2024). Intranasal delivery of LB244-loaded M2 microglia membrane nanoparticles for targeted treatment of neuroinflammation. Advanced Materials, 2419903.
Chen, Y., et al. (2024). Microglia-targeting nanosystems cooperatively delivering herbal ingredients alleviate Alzheimer's disease. Journal of Nanobiotechnology, 22, 433.
Cellfac产品技术资料:BV2小胶质细胞系(小鼠),货号:HY-C024。